I miljöbalken och EU:s lagstiftning definieras en GMO som ”en organism i vilken det genetiska materialet har ändrats på ett sådant sätt som inte sker naturligt genom parning eller naturlig rekombination”. Ofta menas dock en organism i vilken nytt DNA introducerats i genomet med hjälp av rekombinant DNA-teknik.
Mer information finns på sidan GMO-lagstiftningen.

Den genetiska koden DNA fungerar på samma sätt i alla organismer. Det innebär att en ny gen från en organism kan föras in i en annan organisms genom och fungera, det vill säga ge upphov till ett nytt protein. Ett nytt protein kan leda till en ny egenskap.
Ett exempel är Bt-bomull som modifierats med en gen från bakterier av arten Bacillus thuringiensis (Bt). Genen kodar för ett protein som är giftigt för många insekter, bland annat skadeinsekten bomullsmal som kan orsaka stora skördeförluster i en bomullsodling. En odling av Bt-bomull har motståndskraft mot ett angrepp av bomullsmal eftersom malens larver dör när de får i sig proteinet.
Rekombinant DNA-teknik har använts sedan 1970-talet
En ”klassisk” GMO framställs med rekombinant DNA-teknik. Det innebär att nytt DNA, vanligtvis en gen, förs in i en organisms genom. En organism som har en ny gen kallas också för en transgen organism.
Första gången forskare kunde överföra en gen från en organism till en annan var 1973. Då fördes en ny gen in i en bakterie av arten E.coli och fungerade. Forskarna bakom studien var Stanley Cohen och Annie Chang från Stanforduniversitetet och Herbert Boyer och Robert Helling från universitetet i Kalifornien och det väckte stor uppståndelse i forskarvärlden.
Ett år tidigare, 1972, hade en annan forskargrupp, ledd av Paul Berg, utfört ett annat avgörande experiment då de för första gången kopplat ihop DNA från två olika organismer (två virus) och därmed skapat en rekombinant DNA-molekyl. Det blev startskottet för genetisk modifiering.
Genombrotten inom rekombinant DNA-teknik ledde bland annat till ett upprop i den vetenskapliga tidskriften Science. En rad forskare med Paul Berg i spetsen föreslog att allt arbete med rekombinant DNA skulle upphöra tills dess riktlinjer var på plats. Riktlinjerna arbetades fram mellan åren 1973 och 1975 av en grupp med bland annat naturvetare, etiker, jurister och myndighetspersoner.
EU reglerar CRISPR som en GMO
Gensaxen CRISPR/Cas9 är en nyare teknik som utvecklats runt 2010. Den kan användas för att överföra gener men vanligast är att inducera nya mutationer och därmed förändra befintligt DNA. Det kallas för gen- eller genomredigering och inom EU räknas en genomredigerad organism som en GMO och regleras därefter.
Ett trettiotal länder har valt att undanta grödor (och i vissa fall lantbrukets djur) respektive lands ”GMO-lagstiftning”. Inom EU förhandlas ett lagförslag som – om det går igenom – skulle undanta grödor förädlade med till exempel CRISPR/Cas9-teknik EU:s strikta lagstiftning.
Mer information om CRISPR/Cas9-tekniken finns på sidan Gensaxen CRISPR – Gentekniknämnden.
GMO förekommer främst på mikronivå!
Inom många industrier används genetiskt modifierade mikroorganismer (GMMs) till att producera stora mängder proteiner som används i allt från rengöringsprodukter till glass och läkemedel. Till mikroorganismer hör bland annat bakterier, jästsvampar och alger.
Mer information om hur GMMs används finns på sidan Mikroorganismer.
En del läkemedel tillverkas av bakterier
År 1982 blev USA först ut med att godkänna en produkt som tillverkats med GMMs. Produkten var ett läkemedel, insulin, som används för att behandla diabetes hos människor. Innan GMM användes för att tillverka insulin isolerades det från bukspottkörteln hos slaktade kalvar och grisar. Vid den tiden krävdes i storleksordningen 3500 kg bukspottkörtlar från ungefär 24 000 djur för att få fram ett halvt kilo insulin.

Tre år senare godkändes i USA även tillväxthormon. Det hade tidigare isolerats från hypofysen hos avlidna människor, men 1985 upptäcktes en koppling mellan de patienter som behandlats med tillväxthormon och Creutzfeldt-Jacobs sjukdom, en form av galna ko-sjukan. Samma år godkändes det rekombinanta tillväxthormonet.
Koagulationsfaktorer för behandling av blödarsjuka (hemofili) isolerades traditionellt från blodplasma. En koppling till HIV resulterade i att koagulationsfaktorer istället började produceras med hjälp av GMMs. Rekombinant koagulationsfaktor VIII godkändes i USA 1992 och koagulationsfaktor IX 1997.
GMMs hjälper till vid glass- och osttillverkning
Den första produkten som tillverkades av GMM och används vid livsmedelstillverkning var kymosin, ett enzym som gör att mjölk koagulerar vid osttillverkning. Traditionellt används löpe från kalvmagar som innehåller kymosin. Idag produceras produkter som får mjölk att koagulera på både traditionellt vis och via rekombinant DNA.
Under sommaren 2019 lanserades en laktosfri vegansk glass som innehåller samma proteiner som mjölk. För tillverkningen av mjölkproteiner står genetiskt modifierade svampar av släktet Trichoderma. Svamparna har modifierats med gener som kodar för kasein och vassleprotein, som är de huvudsakliga proteinerna i komjölk. Så till skillnad mot produkter som baseras på till exempel sojaproteiner innehåller den här glassen exakt samma proteiner som komjölk, utan att använda kor.
Djur modifieras genetiskt främst inom forskning
Det första genetiskt modifierade djuret var en mus som forskare tog fram 1974. Möss och råttor som används som försöksdjur inom medicinsk forskning är de vanligaste djuren att modifiera genetiskt.
Tusentals avelslinjer med möss har tagits fram som saknar en gen eller ha fått en ny gen. Det är ett sätt att studera geners funktion eller gener som orsakar sjukdomar hos människor. På samma sätt är till exempel genetiskt modifierade råttor och zebrafiskar viktiga inom forskning.
Andra ändamål för genetisk modifierag av djur är att förbättra egenskaperna hos lantbrukets djur, till exempel kor och grisar – men det är inte vanligt förekommande. Inga genetiskt modifierade djur för produktion är godkända inom EU.
Akvariefisk blev första GMO-djuret på marknaden
År 2003 godkändes en självlysande transgen akvariefisk, Glofish, i USA och Taiwan. Fisken hade modifierats med gener från koralldjur och det ursprungliga syftet var att de skulle lysa upp i kontakt med miljögifter, som indikatorer. Av någon anledning fungerade det inte och istället blev de kontroversiella akvariefiskar. Inom EU och större delen av världen är de inte lagligt att ha Glofish.

År 2015 godkände USA det första genetiskt modifierade djuret för livsmedelsmarknaden, en transgen snabbväxande lax som kallas Aqua Advantage. Uppfödningen av laxen avvecklades 2025 på grund av bristande efterfrågan.
År 2020 godkändes en genetiskt modifierad gris, GalSafe, i USA. Grisen får användas både för terapeutiska ändamål och som livsmedel i USA. Den här avelslinjen med grisar har modifierats att inte ha sockermolekylen alfa-gal på ytan av sina celler. Personer som är allergiska mot kött reagerar på alfa-gal och vid xenotransplantation ökar alfa-gal risken för avstötning.
Läs mer om Glofish, AquaAdvantage och Galsafe på sidan om Genetiskt modifierade djur.
Växter kan modifieras med hjälp av en bakterie
På 1980-talet visade forskare att man även kunde modifiera växter genetiskt. I tre vetenskapliga artiklar som publicerades nästan samtidigt demonstrerade tre forskargrupper hur de drog nytta av naturens egen genmodifierare: bakterien Agrobacterium tumefasciens.
I naturen orsakar bakterien A. tumefasciens, en sjukdom som yttrar sig som tumörartade utväxter på den infekterade växten. Bakterierna orsakar det när de modifierar växten genetiskt och för in nya gener i växtens genom. En gen som bakterien för in kodar för ett tillväxthormon vilket gör att de celler i växtens rötter som bakterierna modifierat delar sig okontrollerat. Bakterien för också in gener som kodar för ämnen som kallas opiner som bakterien själv använder som näring. Bakterierna skaffar sig alltså på det här sättet ett eget skafferi.
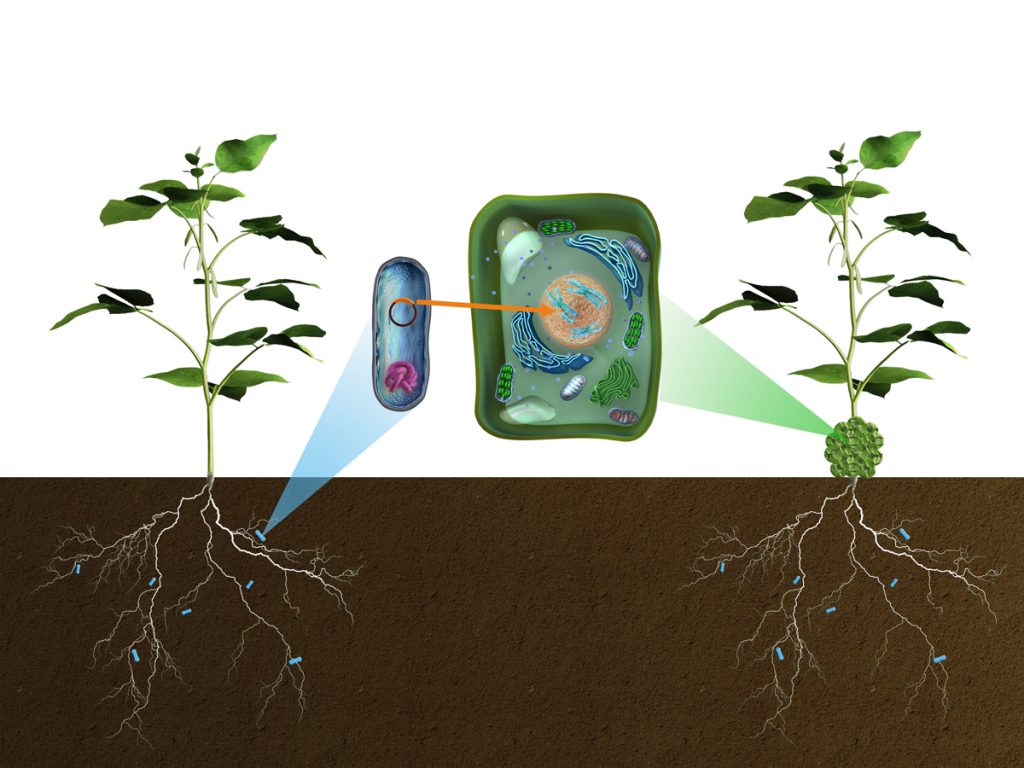
Bakterien nyttjas av forskare för att modifiera växter genetiskt. De byter helt enkelt ut de gener som bakterien vill föra in till de gener som forskaren vill föra in i växten. Bakterien utför ändå arbetet och för in generna i växtens genom.
Sedan dess har andra tekniker för att modifiera växter utvecklats, men forskare tar fortfarande i stor utsträckning hjälp av A. tumefasciens.
Första GMO-växterna på marknaden
Den första genetisk modifierade växt som godkändes som livsmedel var en tomat med fördröjd mognad som kallades Flavr Savr. Den utvecklades i USA och godkändes 1994. Parallellt med Flavr savr-tomaten utvecklade brittiska forskare en tomat med samma egenskap. Tomatpuré från den brittiska tomaten började säljas i Storbritannien 1996.

Sedan 1994 har arealerna med genetiskt modifierade grödor stadigt ökat. Under 2022 odlade 27 länder genetiskt modifierade grödor på totalt 202 miljoner hektar. Odlingsytan motsvarar en femtedel av Europa – men odlingen i Europa utgör en ytterst liten andel. I stället är det Central- och Sydamerika, följt av Nordamerika som har störst areal med genetiskt modifierade grödor. Inom EU har bara en genetiskt modifierad gröda godkänts för odling, en majs som används till djurfoder och den odlas bara i Spanien och Portugal.
Läs mer om genetiskt modifierade växter, vilka som är godkända och var de odlas på sidan Växter.
En genterapi är ett GMO-läkemedel
Det finns en grupp avancerade läkemedel sin innehåller eller består av en genetisk modifierad organism. Ett exempel är genterapier. Det hittills vanligaste förfarandet som används vid de genterapier som används är att celler isoleras från patienten, till exempel ur ett benmärgsprov, och modifieras med en ny gen utanför kroppen (ex vivo).
Genen förs in med hjälp av virus som modifierats genetisk så att det inte kan spridas i kroppen. De genetiskt modifierade cellerna återförs till patienten som behandling.
En behandlingsstrategi är att den nya genen är en ”frisk” gen som kompensera för en muterad ”sjuk” gen. Vid en typ av cancerbehandling som kallas CAR-T-cellterapi förs en ny gen in i patientens immunceller så att de mer effektivt söker upp och dödar cancerceller.
Läs mer om hur genterapier och andra GMO-läkemedel regleras på sidan GMO-läkemedel.
Sidan uppdaterades 2025-05-26
