Introduktion
Vid en cancerbehandling är det ultimata målet att döda cancerceller samtidigt som friska celler skonas. Vårt eget immunsystem är en utmärkt utgångspunkt för detta eftersom vissa immunceller som till exempel T-celler (kallas även T-lymfocyter) och NK-celler (från engelskans Natural Killer cells) kan skilja på friska och sjuka celler.
Utmärkande för cancerceller är att de delar sig okontrollerat och muterar snabbt vilket gör att de tillverkar nya proteiner som kan uppfattas som främmande för immunförsvaret. De proteinerna kallas för neo-antigen.
T-celler har receptorer som känner igen främmande ämnen
För att upptäcka bl.a. cancerceller har T-celler receptorer i sina cellmembran som känner igen och reagerar på antigen som ett ämne som inte hör hemma i den friska kroppen. En antigen kan komma från till exempel en infekterande bakterie eller ett virus eller vara ett neo-antigen som tillverkas av cancerceller.
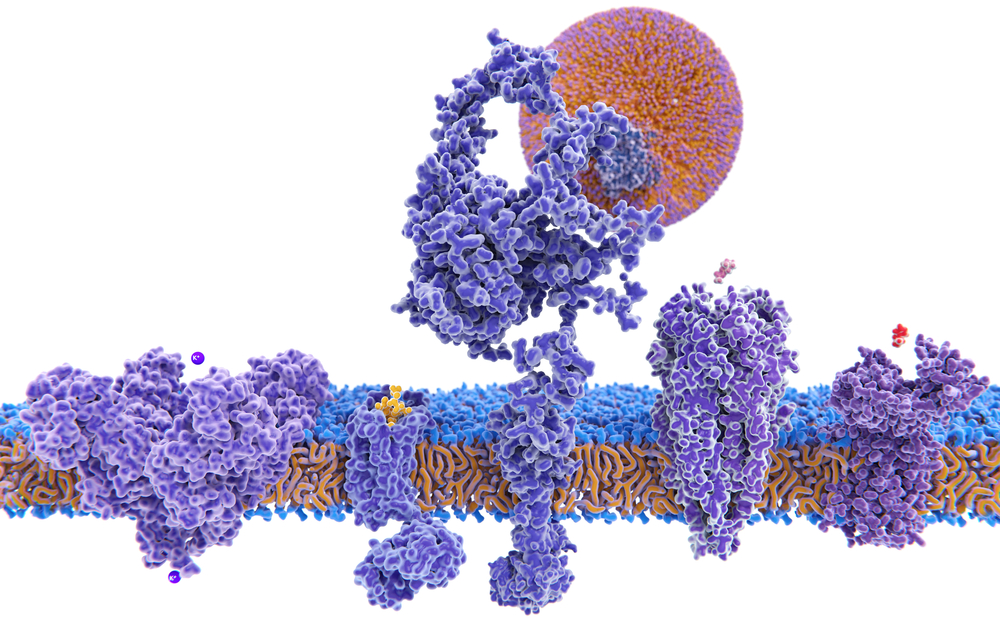
Det finns en annan typ av receptorer som finns på alla friska cellers yta som kallas MHC1. De visar upp delar av cellens innehåll på cellytan och fungerar som en deklaration till T-celler och andra immunceller att allt är lugnt, inget virus eller bakterie har infekterat cellen. Om en cell har omvandlats till en cancercell visar MHC1 ett neo-antigen som T-celler reagerar på och initierar en attack som dödar cancercellen.
NK-celler kontrollerar så att cellerna är friska
Ett sätt för cancerceller att undkomma T-cellerna är att ha färre MHC1-receptorer och därmed visa färre neo-antigen. Immunförsvaret har då en extra kontrollant i form av NK-celler (från engelskans Natural Killer) som reagerar på, och dödar, cancercellen eftersom det inte är friskt att ha så få MHC1-receptorer.
NK-celler reagerar på samma sätt om antikroppar från immunförsvaret har bundit till och ”flaggat” neo-antigen på cancercellernas yta.
Behandlingar som riktar immunförsvaret mot cancern
Både T-celler och NK-celler är viktiga för att förhindra uppkomst och progression av cancer och utgör det immunologiska övervakningssystemet. Cellernas förmåga att upptäcka och döda cancerceller dras nytta av i en typ av cancerbehandlingar som gemensamt kallas cellulära immunterapier.
Behandlingsstrategin är att på olika sätt göra NK- eller T-cellernas reaktion mot cancerceller än mer kraftfull. Ett sätt är att använda genteknik och utrusta cellerna med en nya artificiella receptor som specifik känner igen cancerceller.
Receptorn heter chimär antigenreceptor och förkortas CAR. Behandlingarna kallas därför CAR-T eller CAR-NK beroende på vilken typ av immuncell som modifieras genetiskt med receptorn. CAR-T och CAR-NK räknas både som immunterapier och genterapier eftersom immunförsvaret vänds mot cancercellerna via genetisk modifiering
Flera godkända CAR-T-cellterapier används i Sverige
Ett antal CAR-T-cellterapier är godkända inom EU och några används i Sverige. I några små studier har CAR-T-cellterapier även visats ge god behandlingseffekt för autoimmuna sjukdomar.
Mer information om vilka CAR-T-cellterapier som är godkända finns på sidan Godkända genterapier.
Ännu är ingen CAR-NK-cellterapi godkänts för användning men många är i klinisk prövning.
De CAR-T-cellterapier som är i kliniskt bruk är främst riktade mot B-celler som omvandlats till cancerceller vid olika former av leukemi och lymfom (blodcancer). CAR är då designad att söka upp och döda just B-celler via ett protein på B-celler som heter CD19.
CAR-T-cellerna modifieras på fler sätt än med CAR i syfte att göra dem mer aktiva och att de delar sig snabbare. För dessa justeringar har CRISPR/Cas-teknik visats vara väldigt användbar i behandlingar som är under utveckling.
Dyra men effektiva
CAR-T-cellterapier är avancerade och används bara när andra behandlingsalternativ inte fungerar. Studier visar att behandlingarna i ungefär 40 procent av fallen har en god effekt.
Än så länge har CAR-T-cellterapi använts mest framgångsrikt för patienter med cancerformerna lymfom, akut lymfatisk leukemi och myelom. Det beror på att cancercellerna i dessa sjukdomar har sitt ursprung i B-celler (en annan typ av immuncell). B-celler har unika proteiner på cellytan som inte finns hos andra celltyper. När CAR-T-cellerna riktas mot de specifika proteinerna angrips därför inte andra celler och viktiga organ i kroppen skyddas. Det pågår utveckling av CAR-T-cellterapier mot andra cancerformer, men det har visat sig vara svårare att hitta angreppspunkter för dessa.
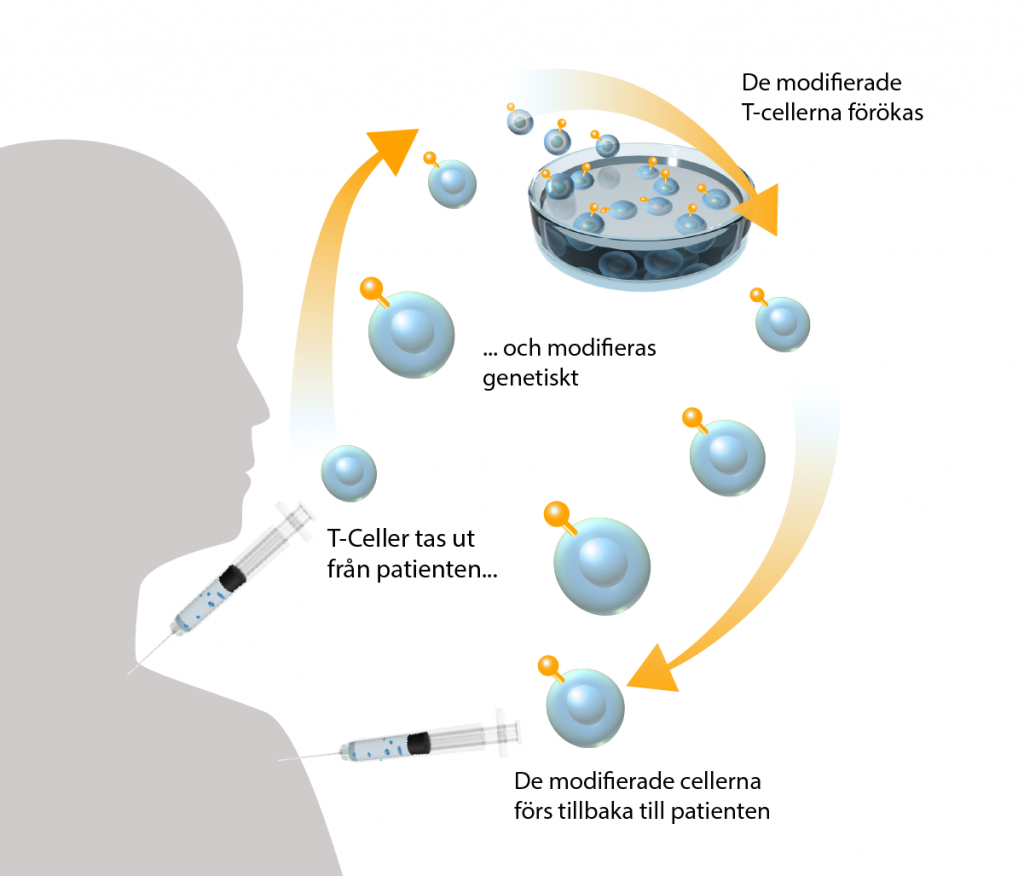
De CAR-T-cellterapier som används i Sverige kostar mellan 3,2 och 3,5 miljoner kronor per dos. Ett sätt att få ner kostanden skulle vara att omvandla CAR-T-cellterapier till en ”off-the-shelf” behandling där en donators celler använts. Många forskare arbetar med att ta fram sådana CAR-T-celler. Förutom att få ner kostanden skulle behandling kunna sättas in snabbare och vara mindre krävande för patienten, än i dagsläget när patientens egna celler behöver isoleras, modifieras och återföras.
Uppdaterad: 2024-05-28

