Möss och råttor är de som används mest inom medicinsk forskning, till exempel för att studera sjukdomar. Det är också oftast möss och råttor som är genetiskt modifierade. Den allra första genetiskt modifierade musen föddes 1974, men det dröjde till början av 1980-talet innan forskare lyckades få till att modifieringen överfördes till avkomman. Det blev starten för hundratals olika avelslinjer där alla möss inom en linje bär på samma genetiska modifiering.
Knock-in, knock-out och transgena möss
Den vanligaste modifieringen hos möss och råttor är att en gen tystas eller ”slås ut”. I Sverige används ofta det engelska uttrycket knock-out för den typen av modifiering. Med en knock-out kan enskilda geners funktion studeras – vad händer i kroppen när inte en viss gen fungerar? Vilka funktioner har genprodukten? Det har varit avgörande för den kunskap vi idag har om geners funktion.
En del gener behövs för att ett liv överhuvudtaget ska utvecklas – och en knock-out är då inte möjlig. Ett alternativ är då att tysta genen i specifika organ eller vävnader. Det kallas för en conditional knock-out.
Det finns också knock-in, där en ny gen först in i genomet. Det kan också vara en befintlig gen som överuttrycks så att det protein genen kodar för tillverkas i större mängd än normalt. En mus som fått en ny gen från en annan art är en transgen. Är genen klonad från människa så säger man också att musen eller råttan är humaniserad.
Sjukdomsmodeller
Genetiskt modifierade möss och råttor används i hög grad som sjukdomsmodeller. Det innebär att de utvecklar en sjukdom, till exempel diabetes eller cancer, som finns hos människa. En genvariant som man vet ger förhöjd risk att utveckla typ 1 diabetes kan till exempel ha förts in i en avelslinje möss. Det ger möjlighet att studera mekanismerna bakom sjukdomen i en biologisk kontext.
Idag finns många olika avelslinjer med genetiskt modifierade möss och råttor. De har visats vara kraftfulla hjälpmedel för att förstå bakgrunden till en mängd olika sjukdomar till exempel schizofreni, diabetes, olika typer av cancer, tarmsjukdomar, inflammation och hjärt-kärlsjukdomar.
Det finns även sjukdomsmodeller som inte är genetiskt modifierade till exempel den så kallade GK-råttan har insulinbrist och utvecklar diabetes. När forskare avlade fram råttan lät de konsekvent de råttor med högst blodsockervärde para sig med varandra. Efter 35 generationer hade de en råtta som spontant fick diabetes.
Varför möss och råttor?
Möss och råttor har använts länge inom medicinsk forskning. Det finns därför mycket kunskap om hur de fungerar och hur de beter sig. Forskare känner också till vilka värden, till exempel blodtryck, kolesterol, insulin, som är normala, vilket underlättar för att dra slutsatser från olika försök. Möss har också liknande organ som oss människor och nästan samma uppsättning gener.
Andra fördelar är att möss är ganska billiga i drift och enkla att sköta om. De förökar sig snabbt och är dessutom inte så känsliga för infektioner. När läkemedel testas behövs också mycket mindre volymer av läkemedlet än om de skulle testas på ett större däggdjur.
Så här modifieras möss och råttor genetiskt
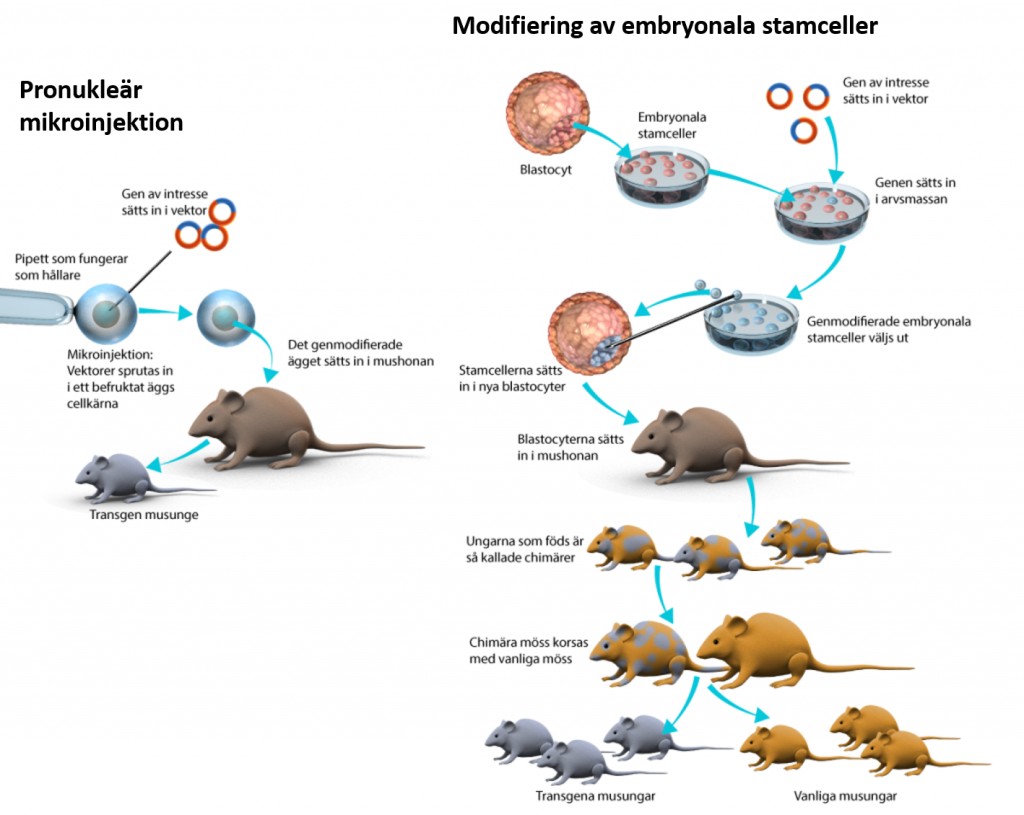
Pronukleär mikroinjektion
Två huvudsakliga metoder används när en genetiskt modifierad mus eller råtta framställs. Den metod som funnits allra längst och fortfarande används är pronukleär mikroinjektion. Metoden går ut på att en vektor med en gen injiceras in i cellkärnan på en nyligen befruktad äggcell, en så kallad zygot. Det görs in vitro. Det befruktade ägget sätts sedan in i livmodern hos en mus- eller råtthona där det utvecklas till ett embryo och vidare till en unge. Metoden är svår och det är lätt att cellkärnan går sönder. Ofta krävs många äggceller för att få till en transgen mus eller råtta.
Embryonala stamceller
Det andra sättet är framställa en genetisk modifierad mus eller råtta är att modifiera embryonala stamceller in vitro. Cellerna tas från en blastocyst som är ett embryo som bara är några dagar gammal. Modifieringen görs med en vektor som innehåller den gen som musen ska modifieras med. De modifierade cellerna förs sedan in i nya blastocyster som har ett vätskefyllt hålrum dit de modifierade stamcellerna injiceras.
Eftersom de är stamceller kan de utvecklas till vilka specialiserade celler som helst. När embryot växer och utvecklas till en unge kommer den att bestå av både modifierade och icke-modifierade celler. Det kallas för chimära möss eller råttor. Några av de modifierade cellerna kan vidareutvecklas till könsceller och modifieringen förs då vidare till nästa generation. Via korsningsscheman kan man få fram möss eller råttor efter några generationer som bara består av genetiskt modifierade celler.
Genomredigerade möss och råttor med CRISPR/Cas9
2013 togs den första genomredigerande musen fram med CRISPR/Cas9. Sedan dess har tekniken revolutionerat även detta område. Framför allt har CRISPR/Cas9 använts för knock-outs, alltså att stänga av gener. Vid genomredigering förs en vektor in med gener som kodar för CRISPR/Cas9-komplexet, det vill säga ett guide-RNA och enzymet Cas9, med hjälp av liknande metoder som beskrivs ovan. Inne i cellerna tillverkas de färdiga komponenterna i CRISPR/Cas9 som aktiverar en förutbestämd redigering.
Tre sjukdomsmodeller med genetiskt modifierade möss
Det finns hundratals olika avelslinjer med genetiskt modifierade möss där alla i samma linje bär på samma genetiska förändring.
Möss med mutationer som ger Alzheimers
Personer med Alzheimers sjukdom har förhöjda nivåer i hjärnan av ett protein som heter amyloid-beta som klumpar ihop sig vid nervtrådarna. Klumparna bildar ett så kallat plack som gör att kontakten och impulserna mellan nervceller blockeras. De symtom som är typiska för sjukdomen som försämrat minne, sämre tidsuppfattning, svårigheter att prata och känna igen det man ser, tros komma från att placket hindrar impulser från att nå hjärnan.
Hos ungefär tio procent av personer som utvecklar Alzheimers tidigt i livet finns mutationer i den gen som kodar för amyloid-beta. Genen heter APP. En musmodell som heter Tg2576 är genetiskt modifierad att efterlikna en patient med Alzheimers. Modifieringen består i att de också har en mutation i APP som gör att de likt Alzheimer-patienter tillverkar förhöjda nivåer av amyloid-beta. Alzheimers beror även på andra orsaker än mutationer i APP, men bildningen av plack är en viktig aspekt av sjukdomen som kan studeras med hjälp av Tg2576.
Studera virusutbrott med humaniserade möss
Möss och människor har ett stort överlapp när det gäller vår uppsättning av gener. Det betyder inte att DNA-sekvenserna eller proteinerna som generna kodar för är exakt samma.
När ett virus infekterar en organism och tar sig in i en cell så görs det via någon av cellens alla yt-receptorer. Viruset är ofta specifikt och behöver en viss receptor, så som den ser ut hos en viss art. Ett virus som infekterar människor brukar därför inte kunna infektera möss eller andra djur.
Infektionssjukdomar kan ändå studeras med möss som modell om den mänskliga gen som kodar för ”rätt” yt-receptor förs in i musens genom. Efter utbrottet 2013 av SARS-Cov (som orsakar SARS) så tog forskare reda på att viruset infekterade celler via en yt-receptor som heter ACE2. Flera musmodeller utvecklades som hade den mänskliga genen av ACE2 för att studera just hur SARS-Cov-viruset fungerar och hur det sprider sig.
Möss utan NOD2 används för att studera inflammation
NOD2 är en gen som kodar för ett protein med samma namn som har en viktig roll för immunförsvaret och för att reglera den inflammatoriska responsen. NOD2-proteinet är en intracellulär receptor, det innebär att den finns inne i cellen och kan ta emot och vidarebefordra signaler.
Det finns särskilda avelslinjer med genetiskt modifierade möss som helt saknar NOD2, har lägre nivåer av NOD2, eller bara saknar NOD2 i något specifikt organ. Med dessa modeller har forskare ökat vår kunskap om hur mutationer i NOD2 kan leda till inflammatoriska sjukdomar. Till exempel forskning visat att utan NOD2 ökar risken att utveckla inflammation i tarmen och kolekteralcancer.
Etiskt tillstånd krävs för att använda försöksdjur
All användning av försöksdjur inklusive genetiskt modifierade möss kräver ett etiskt tillstånd som utfärdas av speciella kommittéer. Det finns sex regionala djurförsöksetiska nämnder i Sverige där varje nämnd består av 14 ledamöter där ordföranden och vice ordföranden är jurister. Resten av kommittén består av forskare, försöksdjurspersonal och lekmän som bland annat representeras av personer från djurskyddsorganisationer.
Andra arter som modifieras genetiskt i syfte att används inom forskning
Andra arter som förekommer genetiskt modifierade i laboratorium är till exempel apor, grisar, bananflugor och zebrafiskar. Bananflugor och zebrafiskar är billiga att använda. Zebrafiskar har dessutom fördelen att de är genomskinliga, vilket gör det möjligt att enkelt följa vad som händer inne i fisken. Det kan vara praktiskt om man till exempel vill testa ett nytt läkemedel för en sjukdom som drabbar hjärnan. Den aktiva molekylen i läkemedlet kan färgas och följas i zebrafisken för att se om den tas upp av hjärnan eller någon annan vävnad.

Grisar används inom ett forskningsområdet som heter xenotransplantation där försök görs att transplantera organ mellan grisar och människa. Ett fåtal försök har gjorts i USA men inte i Sverige. För att mottagarens immunförsvar inte ska stöta bort organet så modifieras grisen genetiskt. Läs mer om det i avsnittet om grisen GalSafe.
Uppdaterad 2024-04-03

